DR EDOUARD PERTUISET - SERVICE DE RHUMATOLOGIE, HOPITAL NOVO, PONTOISE
Nous rapportons ici quelques-unes des très nombreuses communications concernant les maladies inflammatoires, présentées au congrès international 2025 de l’EULAR qui s’est tenu à Barcelone au mois de juin.
Quel choix thérapeutique dans le rhumatisme palindromique ? [Sanmarti R. OP0105]
Le traitement de fond du rhumatisme palindromique (RPA) est empirique et délicat compte tenu de la grande variabilité évolutive. En l’absence d’étude randomisée, l’hydroxychloroquine (HCQ) est le traitement de fond le plus utilisé. L’étude PALABA, étude multicentrique espagnole, randomisée, réalisée en ouvert, a comparé chez des patients ayant un RPA séropositif (facteur rhumatoïde et/ou ACPA), pendant une durée de 24 mois, un traitement par HCQ (5 mg/Kg/j) et un traitement par abatacept (ABA) sous-cutané (125 mg/s pendant 12 mois, puis 125 mg/2s). Dans cet essai, 70 patients (femmes 71 %, âge moyen 51 ans) ont été inclus dans l’analyse en intention de traiter : 34 traités par ABA, 36 traités par HCQ. Le pourcentage de patients ayant terminé les 24 mois de l’étude est de 76 % et 50 % respectivement.
À 24 mois, le pourcentage de patients ayant évolué vers une polyarthrite rhumatoïde (PR ; critères ACR/ EULAR 2010) est de 8,8 z sous ABA (n=3) et de 27,8 % sous HCQ (n=10 ; p=0,047). Chez les patients traités par HCQ, quand une PR s’est développée, ce fut dans les 12 premiers mois dans une grande majorité de cas. À l’inverse, chez les 3 patients traités par ABA et ayant développé une PR, ce fut après 18 mois de traitement.
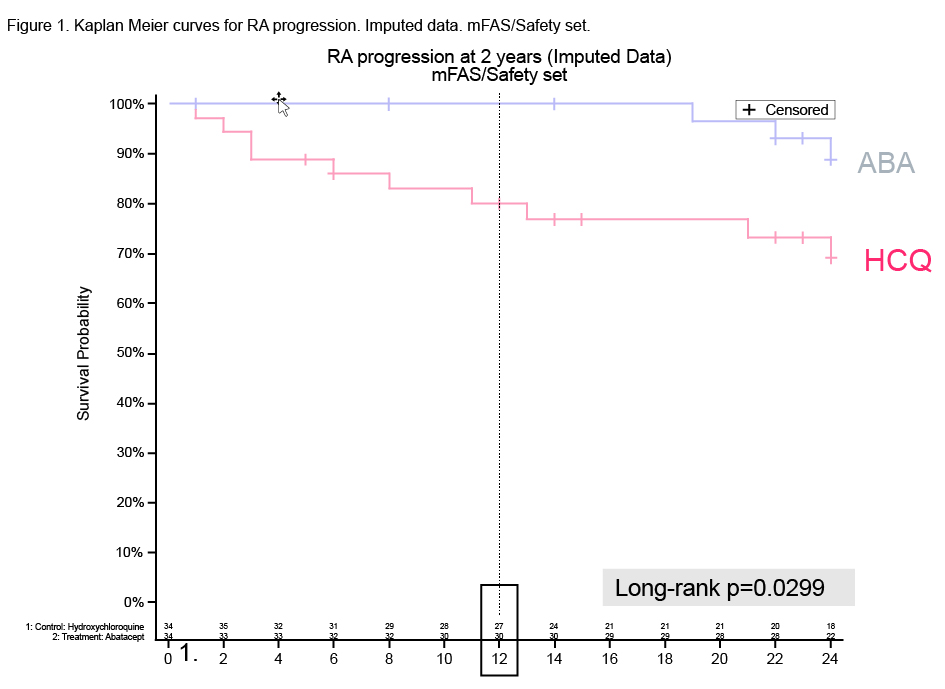
La courbe de Kaplan-Meier montrant la survie sans PR est significative en faveur du traitement par ABA (log-rank test : p=0,029) (Figure 1). Parallèlement, un état de rémission du RPA est observé chez 56 % sous ABA et 23 % sous HCQ (p=0,007).
Cette étude démontre que, chez des patients ayant un RPA séropositif récent (durée moyenne de 10 mois), l’ABA (sans méthotrexate associé) est significativement plus efficace que l’HCQ pour éviter l’évolution vers une PR. Néanmoins, à 24 mois, le taux d’évolution vers une PR n’est que de 28 % sous HCQ, ce qui pose la question : serait-il justifié de traiter par cette biothérapie tous les RPA séropositifs récents ?
Résultats à 5 ans de l’étude TREAT EARLIER dans la pré-PR : un effet du méthotrexate dans les formes sans ACPA [Dumoulin QA. OP0324]
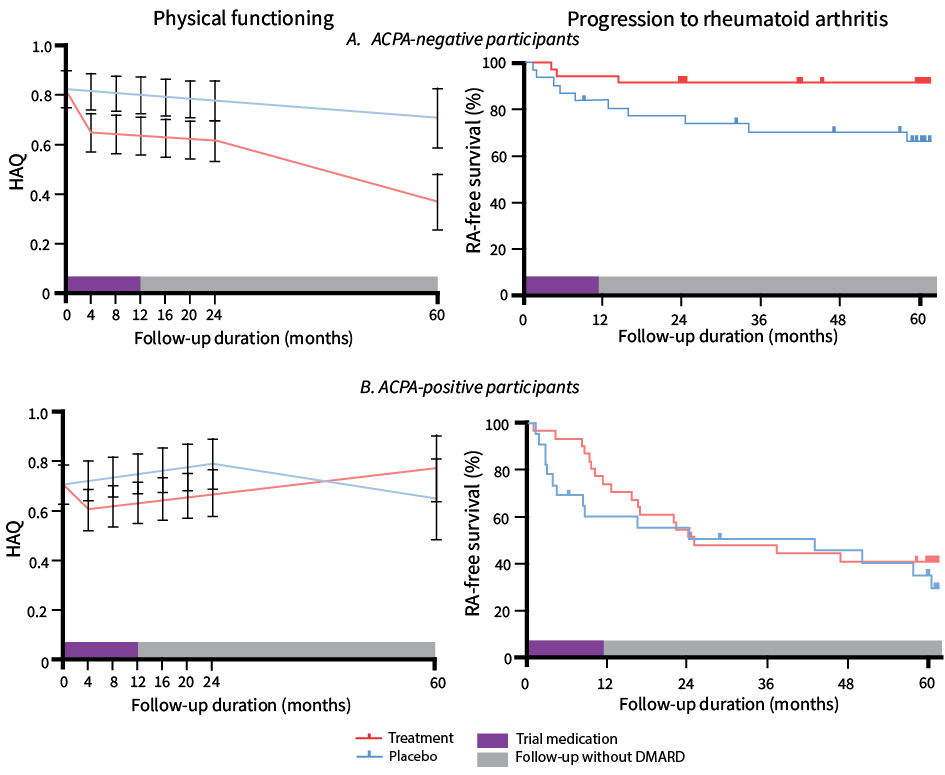
L’étude TREAT EARLIER a inclus des patients ayant une pré-PR à risque élevé de développer une PR : soit ACPA positifs, soit ACPA négatifs avec synovites infracliniques importantes à l’échographie. Elle a comparé un traitement par méthotrexate (MTX ; jusqu’à 25 mg/s) pendant un an et un traitement par placebo (PBO). La communication présentée à l’EULAR présente les résultats à 5 ans, c’est-à-dire 4 années après l’arrêt du MTX. L’analyse comparant MTX et PBO est faite d’une part chez les patients ACPA+ (n=54) et d’autre part chez les patients ACPA- (n=66). Si l’on s’intéresse au risque de développer une PR, il n’y a aucune différence entre les groupes thérapeutiques chez les patients ACPA+ (Figure 2).
Figure 1. Courbe de Kaplan-Meier de la survie sans progression vers une polyarthrite rhumatoïde des patients ayant un rhumatisme palindromique séropositif évoluant depuis moins de 3 ans, traités par abatacept (ABA) ou hydroxychloroquine (HCQ) [Sanmarti OP0105].
En revanche, chez les patients ACPA- et à risque élevé de développer une PR, le risque de développer une PR à 5 ans est de 9 % chez ceux ayant reçu du MTX pendant un an, et de 32 % chez ceux traités par PBO (HR 0,24 ; p=0,018) (Figure 2). L’effet favorable du MTX est également noté
pendant les 5 années sur la capacité fonctionnelle chez les pré-PR ACPA- à risque élevé (Figure 2). Les auteurs concluent à une possible fenêtre d’opportunité dans les pré-PR ACPA- à risque élevé. Néanmoins, les effectifs de l’étude sont modérés, rendant les conclusions incertaines.
|
|
Traitements ciblés et risque de cancer dans la polyarthrite rhumatoïde
Plusieurs communications ont présenté les résultats de registres de vraie vie concernant les risques de cancer chez les patients atteints de PR traités par différentes biothérapies et inhibiteurs de JAK (JAKi).
L’étude JAK-POT regroupe 13 registres nationaux européens et au Québec, de patients atteints de PR et débutant une biothérapie (anti-TNF ou avec un autre mode d’action) ou un JAKi [Aymon R. OP0232].
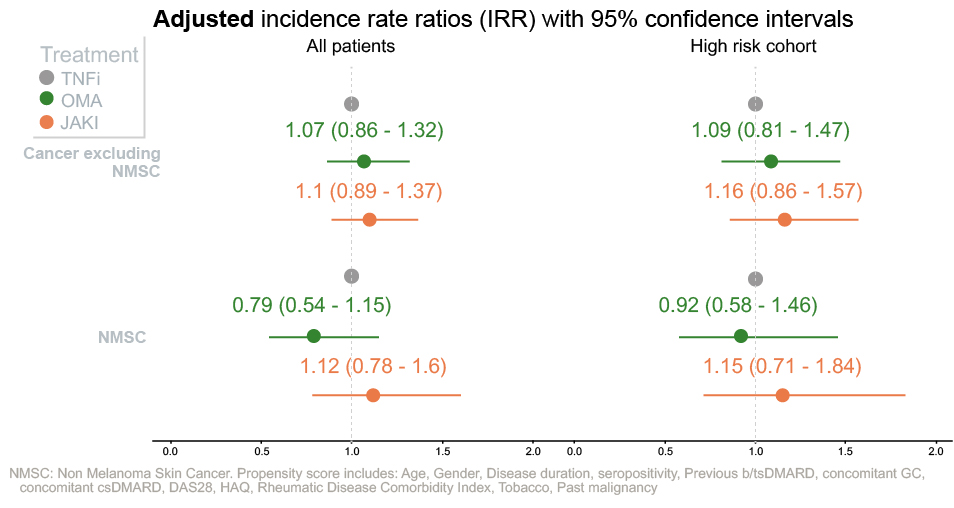
Le but est d’analyser le risque de cancer sous JAKi en comparaison aux anti-TNF et aux biothérapies ayant un autre mécanisme d’action (BIO-AMA). L’analyse comprend 53 169 initiations thérapeutiques chez 33 127 patients. Il a été observé 638 cancers (à l’exclusion des cancers cutanés non mélaniques) et 219 cancers cutanés non mélaniques. L’analyse comparative entre les 3 types de traitements (JAKi, anti-TNF, BIO-AMA), réalisée après ajustement avec un score de propension (prenant en compte les facteurs de risque de cancer), ne montre aucune différence de risque pour les cancers non cutanés et les cancers cutanés non mélaniques (Figure 3). Ceci est vrai dans l’analyse sur l’ensemble des patients, mais aussi sur l’analyse des patients à risque élevé de cancer, qui représentent 35 % de la population de l’étude et qui apparait comparable à la population de l’étude ORAL Surveillance.
Figure 3. Risque de cancers non cutanés (et mélanomes) et de cancers cutanés non mélaniques (NMSC) chez des patients atteints de PR traités par inhibiteur de JAK (JAKi), anti-TNF et biothérapie d’autres mécanismes d’action (OMA) : résultats de l’étude internationale JAK-POT [Aymon R. OP0232].
 |
Le risque de récidive d’un cancer sous un nouveau traitement de fond de la PR a été analysé dans le registre hollandais DANBIO [Westermann R. OP0066]. La moitié des patients inclus avait eu un cancer du sein. Les traitements de fond reçus après la mise en rémission du cancer étaient des biothérapies (n=170), le plus souvent anti-TNF (n=81) et rituximab (RTX ; n=99), ou un traitement de fond conventionnel synthétique (csDMARD,
n=651). Les analyses montrent que le risque de récidive du cancer n’est pas différent qu’il s’agisse des traitements de fond conventionnels synthétiques, des anti-TNF ou du RTX. Ces résultats confirment d’autres données rassurantes concernant les anti-TNF et le risque oncogène. Ceci est encore conforté par l’étude réalisée aux Etats-Unis sur les données de l’assurance maladie (couvrant 48 % de la population) et ayant pour objectif de déterminer l’évolution chez des patients atteints d’une PR, ayant eu un mélanome récent et recevant différents traitements de fond dans l’année suivant le diagnostic [Suarez-Almazor M. OP0068]. Elle a inclus 455 patients (âge moyen 76 ans) répartis en 3 groupes : csDMARD autre que le MTX, MTX, anti-TNF. Dans 95 % des cas le mélanome n'était pas invasif. Il n’est pas observé de différence de la survie entre les 3 types de traitement.
Au total, ces différents résultats s’ajoutent à d’autres, et ne confirment pas ceux de l’étude ORAL Surveillance dont la méthodologie reste a priori la meilleure : s’ils sont rassurants, la prudence s’impose toujours concernant les JAKi en cas de facteur de risque. Ces études et d’autres sont totalement rassurantes pour les anti-TNF, premières biothérapies apparues au début des années 2000, à une époque où la population atteinte de PR était différente, en termes d’activité inflammatoire et de sévérité, ce qui joue un rôle pour la survenue de certains cancers notamment hématologiques.
Caractéristiques des spondyloarthrites axiales difficiles à traiter et réfractaires au traitement : données du registre allemand RABBIT-SpA
[Proft F. OP0098]
L’EULAR a très récemment publié les définitions des spondyloarthrites axiales (axSpA) difficiles à traiter (D2T) [Poddubnyy D. Ann Rheum Dis 2025;84:538-546]. La base de cette définition repose sur l’utilisation d’au moins 2 traitements de fond de mécanisme d’action différent, parmi les biothérapies (anti-TNF, anti-IL17) et les JAKi. Ces définitions distinguent d’abord ce que nous appellerons D2T-axSpA, mais qui est appelé difficile
à « manager », c’est-à-dire à prendre en charge. Ceci est justifié par le caractère en partie subjectif des critères d’évaluation de l’activité inflammatoire de l’axSpA, ce qui peut inciter à des changements thérapeutiques inopportuns.
La D2T-axSpA est définie par au moins un signe (parmi 4 possibles) de contrôle insuffisant de la maladie et la perception problématique de la maladie par le patient et/ou le médecin. Puis, dans cette population de D2TaxSpA, on individualise les axSpA réfractaires caractérisées par l’existence de signes objectifs d’activité : ASDAS-CRP ≥ 2,1 ET, soit inflammation à l’IRM des sacro-iliaques et/ou du rachis, soit CRP élevée.
Les rhumatologues allemands ont utilisé le registre prospectif de patients atteints d’axSpA appelé RABBIT-SpA et ont sélectionné 881 patients ayant débuté une biothérapie ou un JAKi, et pour lesquels ils disposaient d’un recul évolutif d’au moins une année. Parmi ceux-ci, seulement 137 patients (16 %) ont eu au moins 2 biothérapies/JAKi de mécanisme d’action différent. Au total, 75 patients répondent aux critères de D2T-axSPA, ce qui représente 8,5 % de l’ensemble des axSpA incluses dans l’étude. Le groupe des axSpA réfractaire est constitué de 22 patients, ce qui représente 2,5 % parmi les 881 axSpA incluses dans l’étude.
Les auteurs ont comparé les caractéristiques initiales (début du premier traitement) des patients du groupe D2T-axSpA, et aussi celles du groupe axSpA réfractaires, par rapport à celles des axSpA non difficiles à traiter.
Dans le groupe D2T-axSpA, il y a plus de femmes (53 % vs 42 % ), avec un âge un peu plus élevé (45 vs 42,4 ans). Le niveau éducationnel est légèrement inférieur. La prévalence des signes suivants apparait augmentée dans le groupe D2T-axSpA : enthésite (26,7 % vs 17,2 %), arthrite (33 % vs 27 %), évaluation globale du patient (6,8 vs 5,8), BASDAI (5,3 vs 4,6), dépression (6,7 % vs 4,5 %). En revanche, la prévalence des signes suivants semble diminuée : HLA-B27 (68 % vs 77 %), CRP élevée (50 % vs 58 %). Il est notable que ni l’ASDAS, ni le pourcentage d’inflammation à l’IRM (sacro-iliaques ou rachis) ne soient différents. On peut remarquer que ces différences sont faibles et, même si on observe une tendance
à des mesures de PRO plus élevées dans cette population à prévalence féminine plus élevée, il n’apparait pas facile d’individualiser avant le début du traitement les patients qui auront une D2T-axSpA.
Dans le groupe d’axSpA réfractaires, en comparaison avec les axSpA non difficiles à traiter, la prévalence des néléments suivants est augmentée : tabagisme (50 % vs 39 %), enthésite (27 % vs 17 %), évaluation globale du patient (6,8 vs 5,8), BASDAI (5,1 vs 4,6), ASDAS (3,1 vs 2,9), CRP élevée (72,7 % vs 57,7 %), inflammation à l’IRM du rachis (64 % vs 58 %). De manière étonnante, la prévalence du HLA-B27 est diminuée dans cette population (54,5 % vs 77,2 %). Le nombre de patients est ici faible(n=22), ce qui rend difficile les analyses statistiques. Les manifestations extra-articulaires ne semblent pas avoir été analysées comme facteurs prédictifs, mais certains peuvent constituer des biais d’analyse, comme le
psoriasis cutané pouvant favoriser une rotation vers un anti-IL17, ou une maladie inflammatoire colo-intestinale empêchant la prescription d’un anti-IL17.
Les prévalences de la D2T-axSpA et de l’axSpA réfractaire du registre RABBIT-SpA ont été confirmés par les résultats de la cohorte néerlandaise SpA-Net [Smits ML. POS0114] où sur 242 patients, elles étaient respectivement de 9,5 % et 1,7 %. Dans cette étude, le tabagisme actuel et les antécédents de psoriasis cutané étaient des facteurs favorisant l’existence d’une D2T-axSpA. Dans la cohorte turque d’Ankara [Akdemir MC. POS0119], la prévalence de la D2T-axSpA était, parmi 888 patients, de 13,4 %. Dans cette étude, le psoriasis cutané était prédictif de la D2T-axSpA en analyse univariée, mais pas en analyse multivariée.
Au total, en utilisant les définitions de l’EULAR, environ 10 % des patients débutant une biothérapie auraient une maladie difficile à traiter et 20 % de ceux-ci seraient considérés comme réfractaires au traitement. Cette vision correspond-elle à la réalité ? Pour interpréter correctement ces pourcentages, il faut comprendre qu’ils sont fournis par rapport à tous les patients ayant débuté une biothérapie ou un JAKi (dénominateur) mais
que le numérateur exige au moins deux traitements defond de mécanisme d’action différent. Or les anti-TNF ont été très longtemps les seuls, et restent ceux les plus prescrits. Si l’on prend, dans le registre RABITT, comme dénominateur le nombre de patients ayant eu au moins deux traitements de fond de mécanisme d’action différent (n=137), c’est alors 55 % d’entre eux qui ont une D2T-axSpA (75/137), et 16 % (22/137) qui ont une maladie réfractaire, ce qui fait changer la perspective.
Le rhumatisme psoriasique difficile à traiter : les critères du GRAPPA [Proft F. OP0175]
Si les critères des PR et des axSpA difficiles à traiter ont été définis, ce n’est pas encore le cas pour le rhumatisme psoriasique (RPS). Le groupe international d’étude du RPS appelé GRAPPA a donc proposé lors du congrès de l’EULAR des définitions qui sont le fruit d’un travail de consensus, réalisé après analyse de la littérature et des exercices de consensus selon la méthode DELPHI, auprès de 223 professionnels de santé du GRAPPA et de 570 patients atteints de RPS.
Deux entités ont été définies :
1) Le RPS de prise en charge difficile (complex-to-manage psoriatic arthritis) qui regroupe les patients dont la réponse clinique (jugée par le médecin et le patient) n’est pas satisfaisante après au moins un traitement de fond par une biothérapie ou un traitement synthétique ciblé. Cette entité, qui ne nécessite pas la présence de signes objectifs d’inflammation, est en fait un état qui doit parfois faire remettre en cause le diagnostic. L’intérêt de définir cet état est qu’il n’est pas du forcément en rapport avec l’activité du RPS, mais peut être dû à d’autres facteurs comme des comorbidités, des pathologies rhumatologiques associées ou des problèmes d’intolérance médicamenteuse. Cet état, et la qualité de vie dégradée qui s’y rapporte, nécessite donc, de la part du médecin, une analyse de tous les facteurs susceptibles d’y contribuer. Ce type de définition présente un réel intérêt à la fois pratique et théorique, car visant à répondre à cette question : est-ce la maladie ou le malade qui est difficile à traiter ? De plus, cet état est variable et susceptible de disparaître avec une amélioration d’une prise en charge ciblée sur le ou les facteurs causals.
2) Le RPS difficile à traiter ou réfractaire (D2T-RPS) constitue un sous-groupe de l’entité précédente. Les patients sont caractérisés par l’association de 3 éléments :
- ils ont reçu au moins 3 traitements de fond de mécanisme différent, dont au moins 2 biothérapies ou traitement
synthétique ciblé - ils ont des symptômes jugés problématiques par le patient et le médecin
- ils ont au moins un signe objectif d’inflammation du RPS : arthrite, dactylite, enthésite (confirmé par l’imagerie en cas de doute), psoriasis cutané ou unguéal, CRP augmentée (en tenant compte d’autres causes, notamment de l’obésité), atteinte axiale inflammatoire confirmée par l’IRM.
Cette manière d’envisager la difficulté à traiter certains patients est expliquée en partie par la complexité des patients atteints de RPS, mais elle semble également judicieuse pour d’autres rhumatismes inflammatoires chroniques.
Le méthotrexate a-t-il une efficacité dans la pseudopolyarthrite rhizomélique ? [Bolhuis TE. OP0064]
Il existe peu de données sur l’intérêt d’associer un traitement de fond par MTX dans la pseudopolyarthrite rhizomélique (PPR), l’objectif étant en grande partie l’épargne cortisonique. En 2021, une méta-analyse recensait quatre études randomisées comparant le MTX et le placebo, dans lesquelles avaient été inclus au total 194 patients [Song GG. Int J Clin Pharmacol Ther 2021;59:366-371]. Cette méta-analyse concluait à un taux supérieur de rémission avec le MTX et à une dose totale cumulée de prednisone inférieure avec le MTX. Mais il n’existe aucun consensus sur l’utilisation du MTX en dehors des cas de rechute de la PPR, même si certaines recommandations (comme les recommandations norvégiennes) préconisent le MTX chez les patients ayant des comorbidités les exposant particulièrement aux effets indésirables de la corticothérapie [Tengesdal S. BMC Rheumatol 2024;58:4 novembre].De plus, les essais randomisés réalisés ont utilisé de faibles doses de MTX.
Des rhumatologues hollandais ont élaboré un essai thérapeutique contrôlé (PR MODE), randomisé, en double aveugle versus placebo, dont des résultats erronés avaient été présentés au congrès de l’ACR en 2024 (erreurs d’assignation de groupe dans l’analyse statistique).
Les résultats « corrigés » ont été présentés au congrès de l’EULAR 2025. Dans cet essai ont été inclus des patients ayant une PPR (critères ACR/EULAR 2012) récente (les rechutes étaient exclues), traités par corticoïdes depuis moins de 8 semaines. Les patients étaient randomisés dans le groupe PBO ou MTX à la posologie de 25 mg/semaine (durée 52 semaines). Tous les patients recevaient 15 mg/j de prednisolone, qui était diminué progressivement à 0 mg/j au bout de 24 semaines. Le critère principal de jugement était la différence de pourcentage de patients en rémission (PMR-AS < 10) sans corticothérapie à la semaine 52.
L’analyse a porté sur 58 patients : 28 dans le groupe placebo (PBO) et 30 dans le groupe MTX. Les caractéristiques des 2 groupes sont similaires, avec un âge moyen de 63-68 ans et une CRP de 23-26 mg/l en moyenne. Les symptômes de la PPR évoluaient depuis 13-14 semaines. Le pourcentage de patients en rémission sans corticothérapie à S52 est de 80 % sous MTX et 46 % sous PBO : différence de risque 34 %, p=0,0042. Le taux de rechute dans l’année est significativement plus faible sous MTX versus PBO (60 % vs 81 %). Toutefois le dose cumulée de prednisolone à un an n’est pas significativement différente. Il y a une différence non significative dans la fréquence des effets indésirables de grade supérieur
ou égal à 2, en défaveur du MTX.
Au total, il nous semble difficile de conclure compte tenu du faible effectif de l’étude et de l’absence de différence de la dose totale cumulée de corticoïdes. Il est notable que la PPR évoluait en moyenne depuis 3 mois et que le MTX n’a pas été utilisé en sous-cutané, ce qui peut limiter l’intérêt d’augmenter la posologie au-dessus de 15 mg/s. Toutefois, ces résultats peuvent inciter à l’utilisation du MTX dans certaines PPR récentes.
Un anti-TNF pour prévenir les complications obstétricales du syndrome des antiphospholipides [Ware Branch D. OP0273]
Le traitement standard pour prévenir les complications obstétricales du syndrome des antiphospholipides (SAPL) associe l’aspirine à faible dose (ASFD) et une héparine de bas poids moléculaire (HBPM). Dans une cohorte américaine historique de grossesses lupiques, appelée étude PROMISSE et réalisée de 2003 à 2012,le taux d’évènement indésirable (morbidité obstétricale) sévère pouvant être relié à des phénomènes de
thrombose placentaire, était de 37 % (17/46 patientes) chez les femmes ayant un lupus érythémateux disséminé (LED) avec anticorps antiphospholipides, et ce malgré un traitement standard préventif par ASFD et HBPM [Buyon JP. Ann Int Med 2015;163:153-163].
Chez la souris, l’activation de la voie du TNF alpha joue un rôle important dans la survenue d’une dysfonction placentaire (par dysfonction endothéliale) et des phénomènes de thrombose placentaire au cours des complications obstétricales du SAPL. Ceci a été démontré dans des modèles murins de SAPL et de prééclampsie, où l’inhibition du TNF réduit le risque de mort foetale et de retard de croissance, et normalise la taille et la structure du placenta. Ces constatations sont à la base de l’essai thérapeutique IMPACT dont l’objectif a été d’évaluer si le certolizumab pegol (CZP ; anti-TNF ne passant pas la barrière foeto-placentaire), administré au cours de la grossesse chez des patientes ayant un SAPL, en association
à l’ASFD et à l’HBPM, diminue le risque de complications obstétricales du SAPL.
L’étude IMPACT est un essai thérapeutique de phase II, réalisé en ouvert, non contrôlé, chez des patientes ayant un SAPL avec anticoagulant circulant lupique. En l’absence de comparateur, la comparaison a été faite de deux manières : avec les patientes comparables de la cohorte historique PROMISSE (critère principal) ; avec la grossesse antérieure (comparaison intra-patiente) quand cela était possible.
Le traitement par CZP sous-cutané a été prescrit (en association avec ASFD et HBPM) de la 8e à la 28e semaine d’aménorrhée, à la posologie suivante : 400 mg aux semaines S0, S2 et S4, puis 200 mg toutes les deux semaines. Le critère principal d’évaluation est la survenue d’un évènement indésirable sévère (EIS) pouvant être : une mort foetale à 10 semaines et plus, une prééclampsie sévère, une insuffisance placentaire nécessitant un accouchement avant 34 semaines.
Entre mai 2017 et février 2024, 51 patientes ont été incluses dans l’étude. Parmi les 49 patientes ayant eu une grossesse antérieure, 88 % avaient eu un évènement obstétrical sévère. Il est notable que seulement 20 % des patientes ont un lupus systémique associé. Chez les 45 patientes répondant aux critères obstétricaux de SAPL, le taux d’EIS est de 20 % (9/45), ce qui est à comparer aux 37 % de la cohorte historique PROMISSE. Si l’on compare le taux d’EIS chez les 24 patientes ayant eu antérieurement une grossesse au-delà de 10 semaines avec traitement par ASFD et HBPM (n=24), le taux d’EIS est de 21 % dans l’étude IMPACT et de 79 % lors de la grossesse antérieure (p < 0,001).
Ces résultats sont en faveur d’un effet préventif des complications obstétricales du SAPL par l’inhibition du TNF, ceci sous réserve que pour la comparaison avec la cohorte historique PROMISSE, la prise en charge de ces complications s’est améliorée avec les années et qu’il n’est pas certain que les deux populations soient totalement comparables (prévalence différente du lupus associé).
La prescription systématique de l’aspirine à faible dose est-elle bénéfique dans l’artérite à cellules géantes ? [Beydon M. OP0060]
En France, l’aspirine à faible dose (ASFD) est prescrite par certains médecins chez tous les patients ayant une artérite à cellules géantes (ACG), mais les données de la littérature sont contradictoires. Il n’existe pas d’essai randomisé et les recommandations sont plutôt en faveur d’une prescription de l’ASFD chez les patients ayant un risque cardiovasculaire ischémique, mais pas de manière systématique [de Boysson H. Rev Med
Interne 2025;46:12-31]. Il n’en reste pas moins que le risque d’évènement cardiovasculaire ischémique (ECVI) est multiplié par 2 dans l’ACG.
Pour répondre à la question du bénéfice éventuel de l’ASFD dans l’ACG, les auteurs français ont utilisé la base de données du système national des données de santé (SNDS) de l’assurance maladie, afin de comparer les patients atteints d’une ACG ayant reçu de l’ASFD (débutée dans les 14 jours suivant la sortie de l’hôpital), avec ceux n’en ayant pas reçu. Les critères d’exclusion étaient : antécédent de maladie cardiovasculaire, ischémie du nerf optique, traitement récent par ASFD ou anticoagulant. La comparaison est faite entre 4 617 ACG (32 %) ayant reçu de l’ASFD et 9 738 ACG n’en ayant pas reçu (contrôles). Le critère principal est le pourcentage d’évènements cardiovasculaires majeurs (MACE) à 1 an et le bénéfice net fait, qui est le résultat de la balance entre le risque de MACE et celui d’hémorragie grave.
À un an, le pourcentage de MACE n’est pas significativement différent entre les deux groupes (ASFD 3,86 % vs contrôles 4,29 %, p=0,06). En revanche, le risque d’hémorragie grave est significativement plus élevé (+32 %) dans le groupe ASFD. Il n’y a donc pas de bénéfice net de l’ASFD à un an, sous réserve que la mortalité est inférieure à un an dans le groupe ASFD. L’analyse par sous-populations montre que deux sous-populations
bénéficient à un an de l’ASFD : les femmes et les patients diabétiques. Dans ces sous-populations traités par ASFD, le risque de MACE est diminué et le risque d’hémorragie grave n’est pas augmenté. L’intérêt de l’ASFD chez les diabétiques est le même que dans la population générale sans ACG. Le bénéfice de l’ASFD sur les MACE est plus net à 3 ans alors que le risque hémorragique diminue dans le temps, pouvant justifier la prescription
systématique d’ASFD chez les femmes et chez les diabétiques ayant une ACG récente.