ASPECTS GÉNÉRAUX
Les ostéites chroniques récidivantes multifocales sont des affections inflammatoires osseuses, survenant chez des enfants et adolescents, d’étiologie indéterminée, évoluant par poussées alternant avec des périodes de quiescence, pour finir par s’éteindre dans la majorité des cas après quelques années, souvent sans séquelles.
HISTORIQUE
En 1972, Giedion et coll.3 rapportent chez des enfants quatre cas d’ostéomyélites subaiguës et chroniques symétriques. Quelques années plus tard, Probst et coll.9, proposent la dénomination d’« ostéomyélites chroniques multifocales récidivantes ». Les descriptions de cas isolés ou de séries se sont multipliées, dont une large série française de 178 patients en 201514. Les dénominations les plus courantes sont « chronic recurrent multifocal osteitis » (CRMO) et « ostéomyélitechronique récurrente multifocale » (OCRM), mais il y a aussi « ostéomyélite chronique aseptique », « ostéite chronique non bactérienne », etc.
Cette affection présente de nombreux points communs avec le syndrome SAPHO: atteintes inflammatoires lytiques et hyperostosantes et associations avec d'autres pathologies inflammatoires, cutanées en particulier (25 % dans certaines séries d'OCRM, moins fréquemment donc qu'en cas de SAPHO). Il pourrait s'agir d'une seule et même affection dont les manifestations dépendent du degré de maturation du squelette mais cela reste à déterminer6,7. La forme infantile est une atteinte presque exclusivement osseuse tandis que la forme de l’adulte présente une composante d’arthrites plus marquée8.
►ÉPIDÉMIOLOGIE
L'OCRM est une maladie orpheline. L'incidence dans la population pédiatrique était estimée à 1/100.000 dans une série australienne13. L'âge moyen du début de la maladie est de près de 10 ans et le retard de diagnostic de l'ordre de 18 mois dans la large série française14. La prépondérance féminine est très nette : F:H =2:113,14. Au moment du diagnostic, les lésions sont déjà multifocales plus de la moitié des cas. Les localisations les plus fréquentes portent sur les membres inférieurs, puis la clavicule, et plus rarement sur le pelvis, la colonne, la mandibule…3,6,7,9,14. Les localisations articulaires sont rares et plutôt discrètes11,13.
► ANATOMOPATHOLOGIE ET PATHOGÉNIE
L’histologie des lésions osseuses est suggestive d’une ostéomyélite chronique aspécifique, avec un infiltrat inflammatoire lymphocytaire dominant et des signes de remodelage osseux avec épaississement de l’os trabéculaire6,14. Dans certains cas, la prolifération cellulaire peut poser un problème de diagnostic différenciel difficile avec des infiltrations néoplasiques (sarcome d'Ewing ou lymphome par exemple). La pathogénie reste incertaine. L'hypothèse d'une infectionpar un germe peu virulent a bien sûr été discutée3. Les cultures sont parfois positives (surtout proprionibacterium ou staphylococcus). Mais ce sont probablement des découvertes fortuites car les rémissions surviennent de façon équivalente avec ou sans antibiothérapie13,14. Une affection auto-inflammatoire est suggérée par la similitude avec certaines spondyloarthrites et l'association avec certaines affections cutanées inflammatoires. Finalement, la génétique récente fait de l'OCRM un désordre génétique complexe. Des cas familiaux sont rapportés1,12.
►BIOLOGIE
Elle est peu contributive, mise à part un fréquent syndrome inflammatoire, avec une augmentation modérée de la VS (moyenne 35 mm/h) et de la CRP (moyenne 15 mg/l) et une formule sanguine normale13.
►CLINIQUE, ÉVOLUTION, TRAITEMENT
Dans la majorité des cas, le début est insidieux et l’évolution imprévisible consiste en une succession de poussées et rémissions en nombre variable, généralement durant plusieurs années6,14.Selon des séries, les rémissions peuvent être de l'ordre de 90 % à un suivi moyen de 2 ans13 ou de seulement 43 % à un suivi moyen de 4 ans pour des cas plus sévères de centres hospitaliers tertiaires14. La fréquence des manifestations extra-osseuses varie selon les séries (de 12 à 50 %), avec en particulier des
pustuloses palmoplantaires et plus rarement des acnés sévères, des psoriasis ou des maladies de Crohn13,14. Les poussées inflammatoires osseuses et extra-osseuses peuvent être concomitantes ou asynchrones. Les atteintes extra-osseuses peuvent apparaître plusieurs années après les premiers symptômes osseux7. Des associations familiales entre OCRM et autres affections inflammatoires sont observées dans près d'un tiers des cas, principalement avec le psoriasis13,14.
Les anti-inflammatoires par AINS constituent le traitement de première intention, efficace dans une large majorité des cas. Les traitements de seconde ligne sont variés: corticostéroïdes, méthotrexate, sulfasalazine, bisphosphonates, anti-TNFa. Le manque de standardisation reflète l'absence d'essais contrôlés et randomisés14. Le pronostic est donc relativement bon. Mais dans certaines études évaluant l’évolution à long terme (plus de 10 ans), 25 % des sujets présentaient encore une activité inflammatoire persistante et la moitié présentaient des déformations osseuses significatives (d’ordre cosmétique ou asymétrie de longueur des
membres inférieurs)5.
ASPECT EN IMAGERIE
Selon le caractère aigu ou chronique, les modifications osseuses sont un mélange varié d’ostéolyse et d’hyperostose réactionnelle. L’ostéolyse prédomine pendant les phases initiales puis la sclérose et l’hyperostose s'accentuentet deviennent dominants7.
L’hyperostose est caractérisée par un épaississement de la structure trabéculaire et par des appositions périostées qui, avant de se compactiser peuvent présenter un aspect lamellaire suggérant le diagnostic de sarcome ostéogénique ou d’Ewing7,9. En territoire d'os spongieux, les lésions peuvent être purement lytiques, lytiques avec une condensation périphérique, mixtes ou finalement purement condensantes. En territoire cortical, les foyers d'ostéolyse peuvent prendre un aspect microlacunaire perméatif et s'étendre dans les appositions périostées, faisant craindre une lésion plus agressive maligne ou infectieuse en particulier. Mais il n'y a en principe pas d'interruption dans la surface corticopériostée7. Les tissus mous, intramédullaires et périphériques, présentent en phases inflammatoires une infiltration de type oedémateux en hypersignal en IRM avec les séquences sensibles aux liquides, de type pondération en T2, surtout avec suppression du signal de la graisse (« Fat Saturation » ou « T2FS »), ainsi qu'un rehaussement du signal en pondération T1 avec injection de contraste7. Mais il n'y a pas de masse tissulaire tumorale débordant dans les tissus mous périphériques et les anomalies intramédullaires présentent un aspect de type infiltration, moins compact et de limites moins définies qu'en cas de remplacement médullaire par une tumeur. Mais ce sont des séméiologies parfois subtiles.
| APPROCHE EN IMAGERIE |
|
►L’aspect radiologique peut être suggestif mais n'est pas pathognomonique. |
►LÉSIONS OSSEUSES PÉRIPHÉRIQUES
Chez les enfants et les adolescents, les lésions osseuses des membres inférieurs sont les localisations les plus fréquentes, tibias (surtout), fémurs, fibulas3,7,9. Les ostéomyélites chroniques récidivantes multifocales (OCRM) peuvent être symétriques [ibid] (figure 2). Les territoires métaphysaires sont les territoires de prédilection, au contact immédiat des cartilages de conjugaison. Les lésions sont souvent nettement plus étendues transversalement qu’en profondeur. À long terme, les lésions guérissent habituellement sans séquelles: en particulier, les cartilages de conjugaison sont habituellement respectés mais leur fusion prématurée est possible (figure 3), pouvant parfois entraîner des déviations ou des asymétries des membres7. Des lésions similaires se produisent dans d’autres sites: contre les cartilages de croissance des grands trochanters, dans des patellas, des côtes, etc. (figures 1b et 4). En IRM, les anomalies de la moelle osseuses sont plus étendues que celles objectivées par la radiologie standard(figure 5). Par rapport à une ostéomyélite septique, on peut noter l’absence de formation abcédée et, par rapport à une pathologie maligne, le caractère généralement plus limité des lésions intramédullaires et l'absence d'extension tissulaire extra-osseuse7.
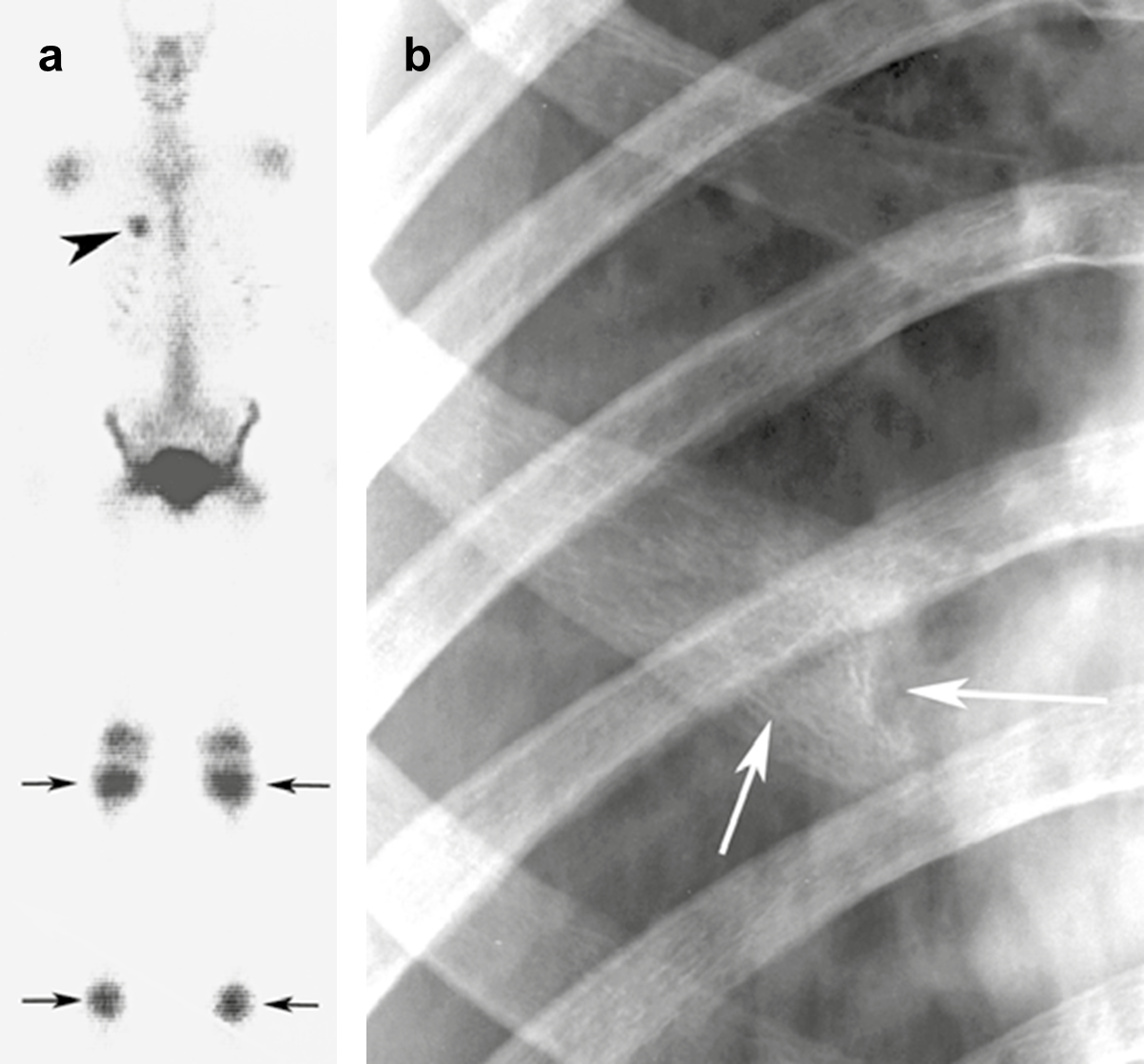
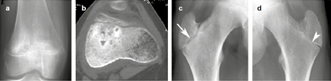
| Figure 1. Intérêt de la scintigraphie. En plus des foyers d’hyperactivité métaphysaire des tibias (flèches), plus marquée que dans les autres métaphyses,la scintigraphie (A) montre un foyer d’hyperactivité costale (tête de flèche). La radiographie (B) y montre un mélange d’ostéolyse et d’hyperostose (flèches) àla jonction chondrocostale augmentant pour ce cas la présomption d'ostéomyélite chronique récidivante multifocale (OCRM) (même patiente que la figure 2). |
 |
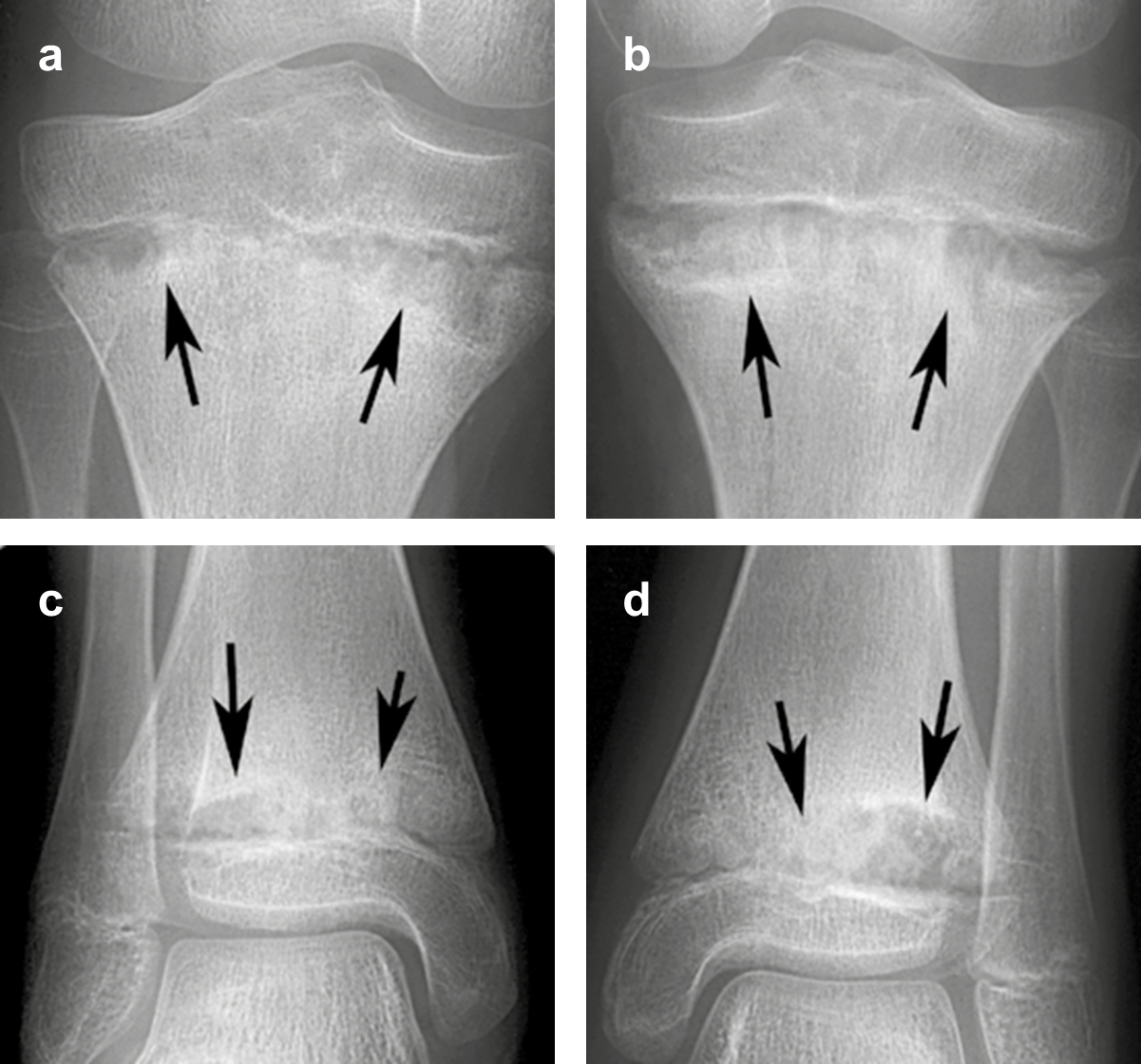
| Figure 2. OCRM de distribution symétrique chez une fillette de 11 ans,avec atteinte des métaphyses tibiales supérieures et inférieures. Les lésions comportent un mélange d’ostéolyse bordée d'hyperostose (flèches) aucontact immédiat des cartilages de conjugaison. |
 |
|
|
|
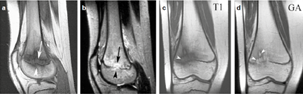
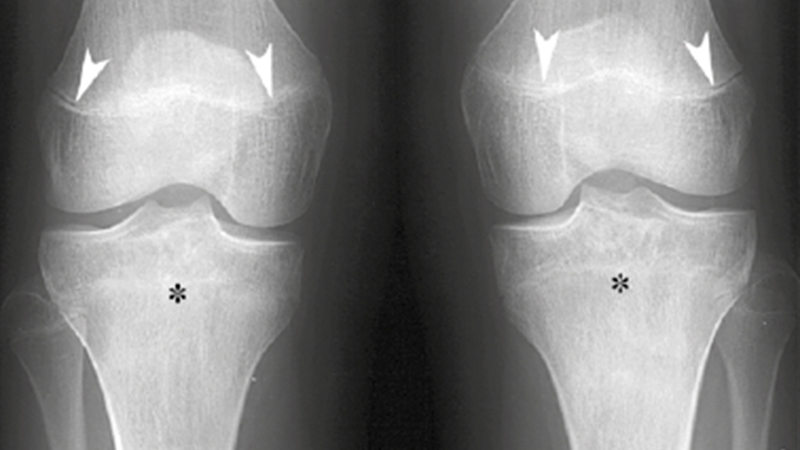
| Figure 6. Localisation diaphysaire chez une jeune fille de 18 ans (évolution de la même patiente que les deux figures précédentes, 4 ans plus tard). Les radiographies standard (A, B) montrent un épaississement cortical surtout sous-périosté (flèches). La vue en plus gros plan (C) montre que l’hyperostose résulte d’appositions périostées à la fois chroniques incorporées à la corticale sous jacente (tête de flèche noire), et aiguës, faiblement calcifiées et avec un aspect lamellaire« en pelure d’oignon » (têtes de flèches blanches). L’IRM sagittale pondérée T1 (D) montre une infiltration très marquée au versant périosté de la corticale diaphysaire antérieure (flèches). Notez que les anomalies métaphysaires présentes sur la figure précédente ont quasiment disparu (astérisque). Des coupes transverses, en pondération T1 et T2 (E et F) montrent que le cortex fémoral est recouvert de couches multiples d’appositions périostées (flèches) en hyposignal sur les deux séquences, entourées d'une infiltration intense de type oedémateux en hypo/hyper signal en T1/T2 (têtes de flèches), et sans modification importante de la cavité médullaire (aspect de corticopériostite plutôt que d’ostéomyélite). |
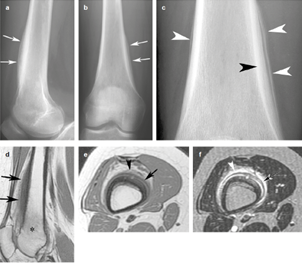
Les lésions diaphysaires (figure 6), plus rares, sont caractérisées par un épaississement cortical plus ou moins étendu résultant d’appositions périostées parfois très épaisses et d'une hyperostose endostéale souvent modérée. L’aspect des épaississements périostés varie selon les phases évolutives : les appositions les plus anciennes sont complètement incorporées à la corticale sous-jacente, tandis qu'en phase aiguë les appositions les plus superficielles, incomplètement ossifiées, sont d'aspect plus flou et présentent parfois un aspect lamellaire et/ou comportant des microfoyers d’ostéolyse. C’est dire si, dans ce cas, les lésions peuvent mimer des affections néoplasiques malignes !
►LÉSIONS ARTICULAIRES
Elles sont plutôt rares et consistent en des mono- ou oligoarthrites transitoires ou récidivantes par poussées5. L’aspect radiologique est habituellement normal ou consiste en un simple gonflement de tissus mous11,13, quoi qu’aient été occasionnellement rapportées des lésions plus destructrices4 (figure 7).
►RÉGION THORACIQUE ANTÉRIEURE
La clavicule est de loin l'os thoracique le plus souvent atteint et représente environ 30 % des OCRM6,7,9. C’est en fréquence la deuxième localisation d'OCRM après les métaphyses des membres inférieurs2,9. La lésion débute dans la portion médiale de la clavicule par une lésion qui initialement peut être purement lytique, avec une infiltration de type oedémateux souvent intense en IRM7 (figure 8).
| Figure 7. Atteinte articulaire : Chez une jeune fille de 16 ans dont l'ostéite de la clavicule évoluait depuis de nombreuses années (même patiente que celle de la figure 9, voir plus loin), la radiographie (A) des doigts montre une tuméfaction des tissus mous au voisinage de l’IPP de l’annulaire (tête de flèche). Un an plus tard (B), une arthropathie plus destructrice s’est développée au niveau de l'IPD du même doigt (flèche). |
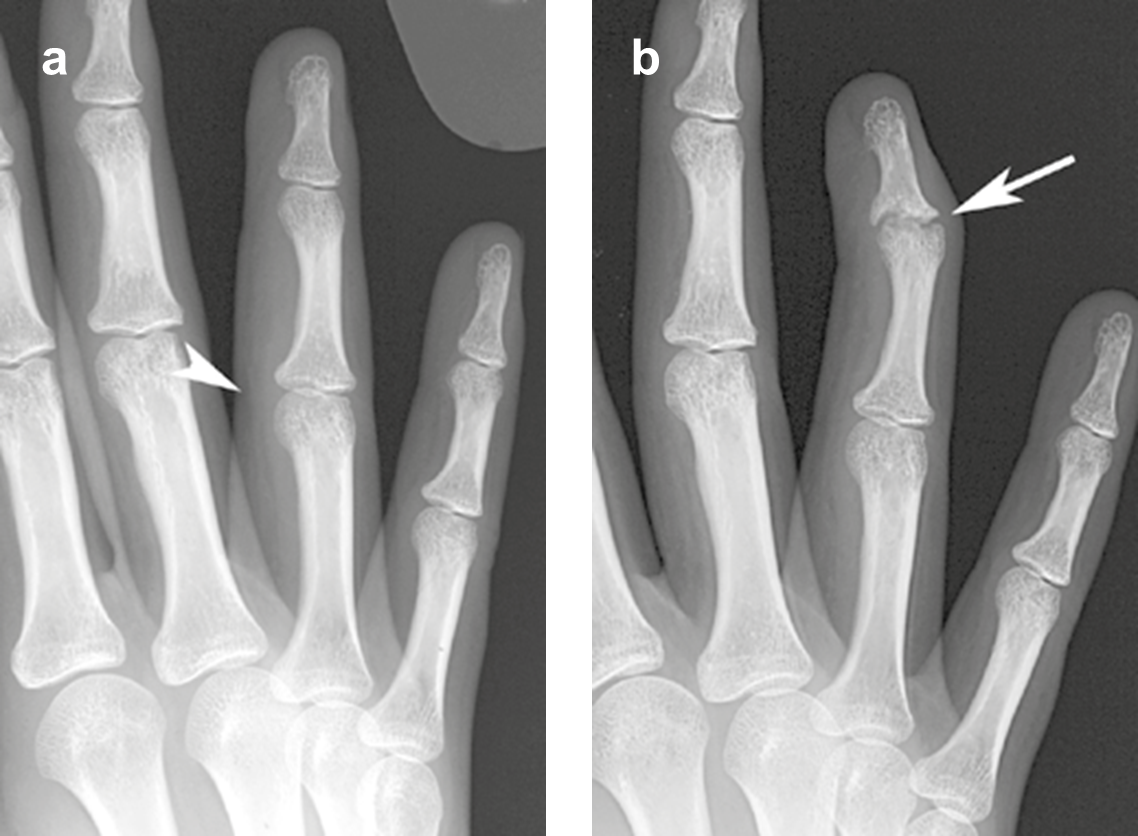 |
| Figure 8. Ostéite claviculaire aseptique en phase subaiguë chez une fillette de 11 ans. A: La radiographie montre un foyer d'ostéolyse dans la tête claviculaire (flèche) avec une hyperostose périphérique floue s'étendant sur plusieurs cm latéralement (têtes de flèches). B : L'IRM en T2FS montre une importante infiltration en hypersignal de type oedémateux dans et autour de cette portion claviculaire (flèches). C : Quinze mois plus tard (après traitement par bisphosphonates), l'infiltration de type inflammatoire a nettement régressé. D : Mais quatre ans plus tard, une autre lésion est apparue dans la métaphyse inférieure d'une fibula (flèche) avec une infiltration des tissus mous adjacents (astérique) bien visible sur cette IRM pondérée T2FS. |
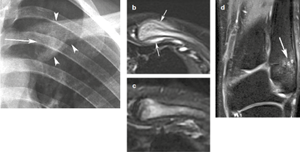
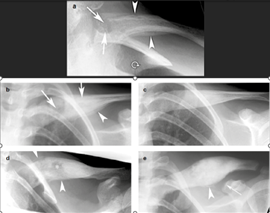
Le diagnostic différentiel avec d’autres lésions est, à ce stade, parfois quasi impossible (versus sarcome d'Ewing, histiocytose langerhansienne ou ostéomyélite bactérienne aiguë par exemple). Puis, l’ostéolyse et l’hyperostose s’associent pour former un remaniement hétérogène comportant un aspect micro-lacunaire, une densification interne mal structurée et des appositions périostées, qui peuvent être d’aspect lamellaire avec même des aspects de triangles de Codman pendant les poussées évolutives3 (figure 9). Au cours de son évolution, l’ostéite migre lentement latéralement, tandis que le segment interne peut retrouver une structure osseuse plus normale7. À long terme,le processus hyperostosant peut entraîner un épaississement considérable de la clavicule7 (figure 9e). À noter qu'il n'y à pas d'atteinte articulaire, à l'inverse des localisations de SAPHO du même territoire7. D’autres atteintes plus rares peuvent porter sur d’autres localisations de la cage thoracique, par exemple sur les jonctions chondrocostales (figure 1b).
►ATTEINTES VERTÉBRALES
Elles sont relativement rares et portent habituellement sur une seule vertèbre10. Elles sont caractérisées en phase initiale par une ostéolyse avec collapsus vertébral partiel ou complet2, posant le diagnostic différentiel avec une lésion néoplasique maligne, une histiocytose langerhansienne ou une spondylodiscite infectieuse. Contrairement aux spondylodiscites, il n’y a pas de destruction de disques intervertébraux7,9.
|
Puis, l’hyperostose intracorporéale l’emporte très largementsur les lésions lytiques, posant le diagnostic différentiel d’avec des « vertèbres d’ivoire » néoplasiques11.
►RÉGIONS PELVIENNES ET AUTRES
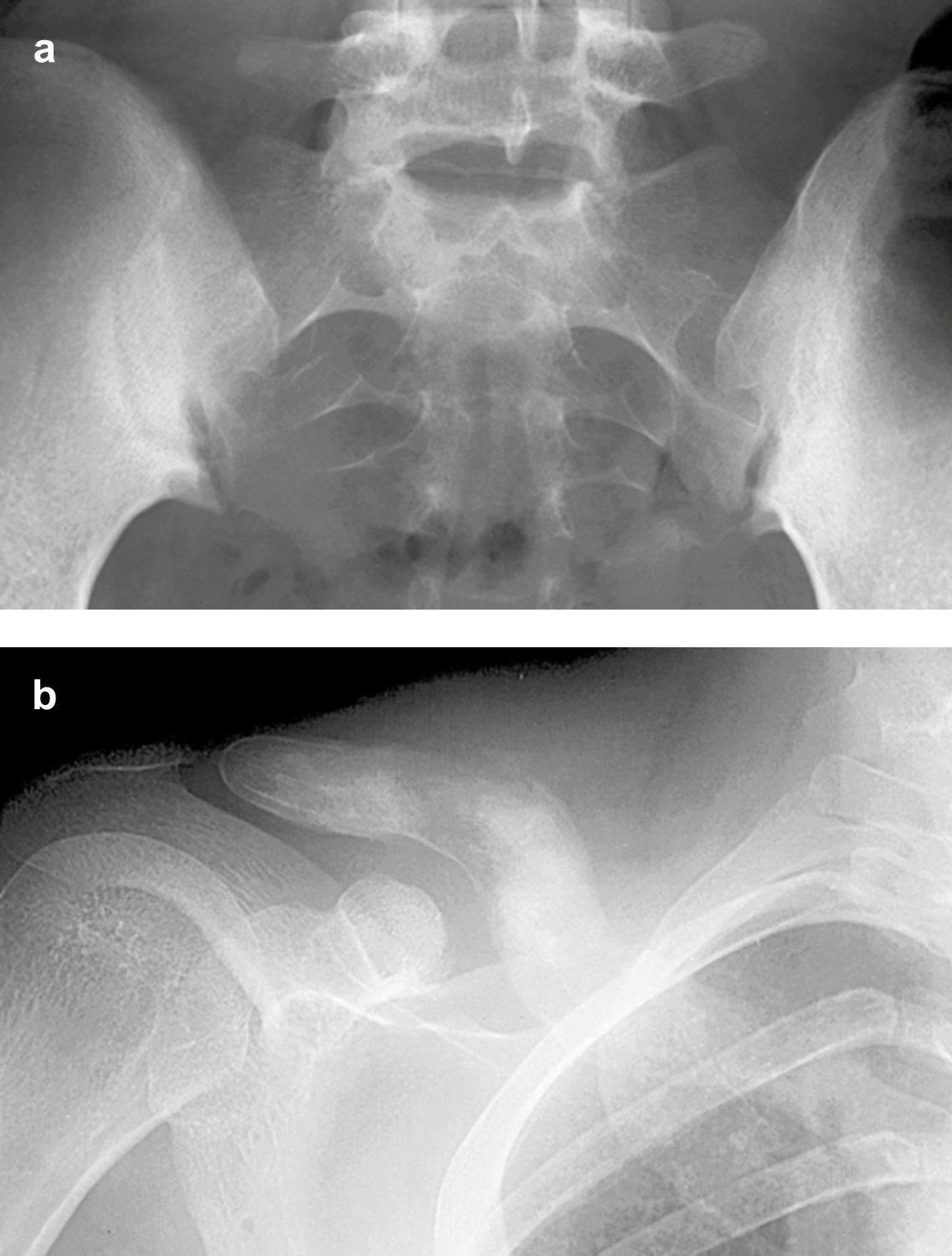
L’atteinte des articulations sacro-iliaques se caractérise par les mêmes types de lésions élémentaires: ostéolyse sous chondrales et hyperostose plus ou moins étendue (figure 10). L’atteinte est généralement unilatérale et porte souvent, comme le SAPHO, sur une seule berge articulaire7,8. D'autres localisations pelviennes sont décrites dans le voisinage des synchondroses ischio pubiennes ou dans les ailes iliaques7. La mandibule est un autre site rare, 2 à 5 % selon des séries14.
| Figure 10. Atteinte sacro-iliaque bilatérale (A) caractérisée par des érosions et une hyperostose de voisinage, chez une jeune fille de 16 ans dont l’ostéite claviculaire (B) évoluait depuis le nombreuses années (NB: comme chez sa soeur jumelle). |
 |
| CONCLUSION |
| • Le diagnostic d’ostéomyélite chronique récurrente multifocale reste essentiellement un diagnostic d’exclusion. • L’aspect peut être caractéristique mais pas spécifique. • Le diagnostic différentiel se pose, de façon variable selon les phases évolutives avec de multiples autres affections, infectieuses et néoplasiques en particulier. • D’où un intérêt majeur à rechercher les localisations multiples éventuellement occultes, par scintigraphie ou IRM corps entier, et à disposer, chaque fois que cela est possible, de documents antérieurs permettant de montrer l’évolution caractéristique des lésions. • Les examens en IRM (surtout) et en TDM, sans non plus être spécifiques, peuvent apporter des éléments importants dans le diagnostic différentiel, en montrant en particulier une absence de lésion abcédée ou de formation tumorale caractérisée. • La biopsie est nécessaire dans les cas douteux.d’ostéomyélite chronique récurrente multifocale reste essentiellement un diagnostic d’exclusion. • L’aspect peut être caractéristique mais pas spécifique. • Le diagnostic différentiel se pose, de façon variable selon les phases évolutives avec de multiples autres affections, infectieuses et néoplasiques en particulier. • D’où un intérêt majeur à rechercher les localisations multiples éventuellement occultes, par scintigraphie ou IRM corps entier, et à disposer, chaque fois que cela est possible, de documents antérieurs permettant de montrer l’évolution caractéristique des lésions. • Les examens en IRM (surtout) et en TDM, sans non plus être spécifiques, peuvent apporter des éléments importants dans le diagnostic différentiel, en montrant en particulier une absence de lésion abcédée ou de formation tumorale caractérisée. • La biopsie est nécessaire dans les cas douteux. |
RÉFÉRENCES
► 1. Cox AJ, Ferguson PJ. Update on the genetics of nonbacterial osteomyelitis in humans. Curr Opin Rheumatol. 2018; 30: 521-525.►2. Cyrlak D, Pais MJ.Chronic recurrent multifocal osteomyelitis. Skeletal Radiol 1986, 15: 32-39.►3. Giedion A, Holthusen Giedion A, Holthusen W, Masel LF, Vischer D. Subacute and chronic « symmetrical » osteomyelitis. Ann Radiol 1972, 15 : 329-342.►4. Huaux JP, Maldague B, Malghem J, Meunier H, Noel H, Nagant de Deuxchaisnes C. Pustulotic arthroosteitis and related disorders in children and adults. J Belge Radiol 1986, 69: 345-354.►5. Huber AM, Lam PY, Duffy CM et al. Chronic recurrent multifocal osteomyelitis : clinical outcomes after more than five years of follow-up. J Pediatr 2002; 141 : 198-203. ►6. Jurik AG, Helmig O, Ternowitz T, Moller BN.Chronic recurrent multifocal osteomyelitis : a follow-up study. J Pediat Orthop 1988, 8: 49-58. ►7. Khanna G, Sato TS, Ferguson P. Imaging of chronic recurrent multifocal osteomyelitis. Radiographics. 2009; 29:1159-77.►8. Malghem J, Vande Berg B, Lebon C, Maldague B. Spondylarthropathies et affections apparentées. In: Imagerie ostéo-articulaire. Pathologie générale. JD Laredo, G Morvan, M. WybierEds. Flammarion. Paris.1998; 413-453. ►9. Probst FP, Björksten B, Gustavson KH. Radiological aspect of chronic recurrent multifocal osteomyelitis. Ann Radiol 1978, 21: 115-125. ►10. Quelquejay C, Job-Deslandre C, Hamidou A, Benosman A, Adamsbaum C. Ostéïte chronique multifocale récurrente de l’enfant. J Radiol 1997; 78: 115-121. ►11. Resnick D., Niwayama G. Enostosis, hyperostosis and periostitis. In D. Resnick (Ed) : Diagnosis of bone and joint disorders, W.B. Saunders Company, Philadelphia, 4rd edition, 2002, pp 4844-4850. ►12. Taddio A, Zennaro F, Pastore S, Cimaz R. An Update on the Pathogenesis and Treatment of Chronic Recurrent Multifocal Osteomyelitis in Children. Paediatr Drugs. 2017; 19:165-172.►13. Walsh P, Manners PJ, Vercoe J, Burgner D, Murray KJ. Chronic recurrent multifocal osteomyelitis in children: nine years' experience at a statewide tertiary paediatric rheumatology referral centre. Rheumatology (Oxford). 2015; 54:1688-91.►14. Wipff J, Costantino F, Lemelle I et al. A large national cohort of French patientswith chronic recurrent multifocal osteitis. Arthritis Rheumatol. 2015;





