LES RHUMATISMES INFLAMMATOIRES CHRONIQUES AU CONGRÈS DE L’EULAR 2022
DR EDOUARD PERTUISET - SERVICE DE RHUMATOLOGIE, CENTRE HOSPITALIER RENÉ DUBOS, PONTOISE
Nous présentons ici la suite des comptes rendus du congrès européen de l’EULAR qui s’est déroulé en juin 2022 à Copenhague, en livrant la deuxième partie consacrée à
la polyarthrite rhumatoïde et celle consacrée à la spondyloarthrite axiale.
| POLYARTHRITE RHUMATOÏDE : 2e PARTIE |
Corticothérapie à faible dose dans la PR du sujet âgé : étude GLORIA
L’utilisation d’une faible corticothérapie dans la polyarthrite rhumatoïde (PR) du sujet âgé est classique, mais son rapport bénéfice/risque n’est pas bien connu à l’ère des traitements de fond conventionnels ou ciblés. L’étude GLORIA [M. Boers. OP0263] est une étude internationale européenne dont l’objectif était d’analyser le rapport bénéfice/risque d’une corticothérapie à faible dose (prednisolone 5 mg/j) chez des patients âgés de 65 ans et plus, et nécessitant un ajustement du traitement de la PR (DAS28 ≥ 2,60). Il faut souligner d’emblée plusieurs éléments :
• il ne s’agit pas de PR récente : ancienneté moyenne 11 ans ;
• il s’agit de PR destructrices (96 % des patients) ;
• le traitement de fond a rarement été changé à l’inclusion (14 %) ;
• l’essai a été mené en partie pendant la pandémie de la COVID-19 ;
• seulement 60 % des patients environ ont terminé les 2 ans de l’étude.
Il s’agit d’un essai pragmatique, randomisé, en double insu, de la prednisolone versus placebo. Au total, 449 patients ont été traités, soit par prednisolone 5 mg/j, soit par placebo, en supplément d’un traitement de fond (79 %), ou sans traitement de fond. Mais des modifications du traitement de fond étaient autorisées pendant l’étude.
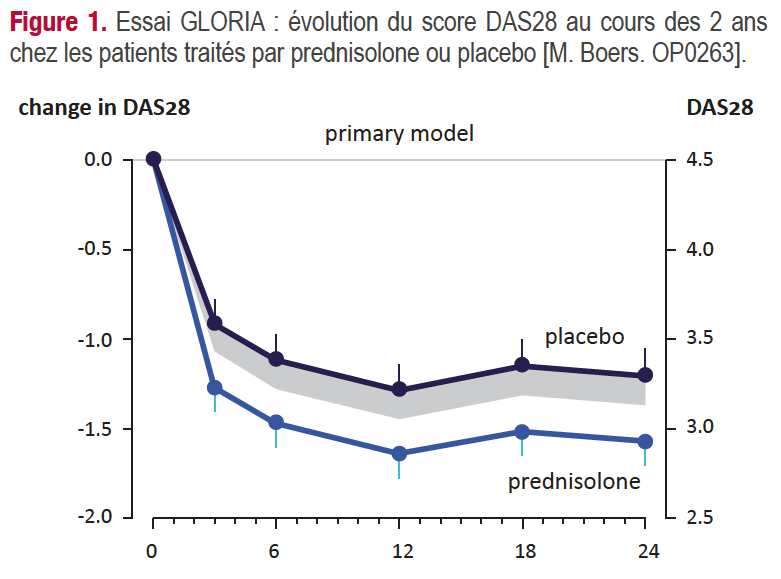
Concernant l’évolution de l’activité de la PR (score DAS28 initial 4,5 en moyenne), l’amélioration du score DAS28 est significativement plus importante sous prednisolone dès 3 mois, à un an et à 2 ans (p < 0,0001) (Figure 1). Toutefois dans un modèle ajusté en fonction des changements du traitement de fond, la différence qui persiste à un an, disparait à 2 ans. À 2 ans, la progression structurale radiographique (score de Sharp modifié par van der Heijde) est significativement inférieure dans le groupe prednisolone vs placebo (p=0,02).
 |
L’analyse des effets indésirables sous traitement est importante. Pendant les 2 ans, le taux des effets indésirables sévères a été numériquement supérieur dans le groupe prednisolone vs placebo : 23 vs 18 p. 100 patients-année. Le principal effet indésirable ayant été plus fréquent sous prednisolone était l’infection. Le taux d’infection sévère était de 7,3 vs 4,5 pour 100 patientsannée (prednisolone vs placebo). En revanche il n’y avait pas de sur-risque pour les fractures symptomatiques, l’HTA, le diabète, la cataracte.
Au total, l’intérêt d’une corticothérapie à faible dose pour diminuer l’activité de la PR chez ces patients âgé de 65 ans et plus, est démontré. La question principale est celle de la toxicité. La toxicité métabolique n’apparait pas ici mais le suivi est faible (2 ans). Néanmoins, même avec ces faibles doses, les infections sévères sont plus fréquentes. Ces résultats nous confortent dans une utilisation raisonnée de la corticothérapie chez ces patients, qui ne doit pas remplacer l’intérêt essentiel de l’optimisation des traitements de fond dans la PR y compris après 65 ans
Risque de nouveau cancer chez les patients PR avec antécédent de cancer et traités par une biothérapie ou anti-JAK : résultats du registre espagnol BIOBADASER
Le risque de nouveau cancer chez un patients atteint d’un rhumatisme inflammatoire chronique (RIC) et chez lequel on débute un traitement par biothérapie ou inhibiteur de JAK (JAKi) reste une question difficile dans la mesure où ces patients ont été exclu des essais thérapeutiques. Les décisions restent délicates en pratique, même si historiquement l’utilisation du rituximab a été privilégiée du fait des données antérieures rassurantes avec ce médicament utilisé dans les hémopathies malignes. Certaines données sont rassurantes avec les anti-TNF, mais la pratique doit absolument prendre en compte le type et l’ancienneté du cancer. De plus, pour les JAKi, les résultats de l’étude ORAL surveillance chez les patients âgés traités avec le tofacitinib doivent rendre prudent. Les données de vie réelle, provenant des registres, sont donc très utiles.
Les résultats concernant le registre espagnol BIOBADASER ont été rapporté à ce congrès [J Molina Collada.
OP0138]. Parmi les 9 129 patients atteints d’un RIC dans BIOBADASER (traitement par biothérapie ou JAKi), 352 avaient un antécédent de cancer (cancer solide, mélanome, hémopathie maligne). Ces patients ont été traités par : anti-TNF (n=185), JAKi (n=61), anti-CD20 (n=61), anti-IL6 (n=68), anti-CTLA4 (abatacept, n=47), anti-IL17 (n=39). L’analyse compare le taux d’incidence d’un nouveau cancer entre les différents traitements avec pour référence les anti-TNF.
Chez les 352 patients, il y a eu 32 cancers incidents : 17 cancers solides, 14 cancers cutanés non mélaniques, 1 mélanome. L’analyse est faite sur l’ensemble de ces cancers (cutanés et d’organe). L’incidence chez les patients traités par anti-TNF est de 38,3 pour 1 000 patients-année (P-A). Le ratio d’incidence pour chaque traitement en comparaison avec les anti-TNF est de : 0,6 (IC95 : 0,1-2,5) pour les JAKi ; 0,3 (IC95 : 0,1-1,4) pour les anti-CD20 ; 1,2 (0,5-3,4) pour les anti-IL6 ; 1,3 (0,5-3,6) pour l’abatacept (non évaluable pour anti-IL17 car pas de cas de cancer incident). Ici, il n’apparait donc pas de différence significative entre les différentes biothérapies et JAKi.
Cette analyse peut être critiquée car :
• le nombre de patient est faible pour une telle étude;
• il y a peu de cancers solides non cutanés ;
• la comparaison ne tient pas compte (absence d’ajustement) des autres facteurs de risque cancéreux et du type de cancer antérieur.
On peut en conclure que, si différence il y a entre ces traitements, elle n’est pas majeure. En pratique, le type de cancer (organe, diffusion) et son ancienneté sont des éléments majeurs de la décision (conjointe avec un oncologue) dans cette situation.
Effet défavorable de la corticothérapie au cours de la grossesse dans la polyarthrite rhumatoïde : résultats de la cohorte GR2
La cohorte GR2 est une cohorte française prospective observationnelle des grossesses survenant chez les patientes atteintes de maladies inflammatoires rhumatologiques ou systémiques. Cette analyse de patientes PR de la cohorte GR2 avait pour objectif de déterminer les facteurs associés à une grossesse d’évolution défavorable (au sens obstétrical du terme) au cours de la PR [S. Hamroun. OP0127]. La grossesse favorable est un indice composite associant : accouchement à terme (≥ 37 semaines) d’un enfant vivant et en bonne santé avec poids de naissance supérieur au 10° percentile.
Dans cette analyse où ont été inclus 92 grossesses, un des traitements suivants a été pris au moins une fois au cours de la grossesse : corticostéroïdes 46 %, AINS 8 %, biothérapie 43,5 %. Une fausse couche est survenue dans 10 % des cas. Dans 83 % des cas (n=69) la patiente a accouché à terme d’un enfant vivant.
Une évolution défavorable de la grossesse est survenue dans 43,5 % des cas, liée principalement à la prématurité (17 %) et à un poids insuffisant pour l’âge gestationnel.
Dans une analyse multivariée, les facteurs suivants étaient associés à cette évolution défavorable : l’âge, la nulliparité et la prise de corticostéroïdes. L’odds ratio de la corticothérapie (au moins une fois, dose non précisée) était de 3,22 (IC95 : 1,09-9,6 ; p=0,04). Ce résultat incite à ne pas prescrire de corticothérapie au cours de la grossesse dans la PR, venant s’ajouter aux risques pour la mère. Il est notable que l’activité de la PR (DAS28-CRP > 3,2 au moins une fois : chez seulement 22 % des patientes) n’était pas corrélée avec l’évolution de la grossesse.
Risque d’événements cardiovasculaires majeurs dans la polyarthrite rhumatoïde traitée par inhibiteur de JAK : résultats du registre allemand RABBIT
La tolérance des inhibiteurs de JAK (JAKi) dans la PR a été remise en question par les résultats de l’étude randomisée ORAL surveillance où, chez les patients à risque (≥ 50 ans et au moins un autre facteur de risque cardiovasculaire) traités par tofacitinib (résultat poolé des 2 posologies 5 et 10 mg x 2/j), le risque de survenue d’un évènement cardiovasculaire majeur (appelé MACE) est significativement augmenté de 33 % par rapport aux patients traités par anti-TNF [Ytterberg SR. N Engl J Med 2022 ; 386 : 316-26]. Dans le large registre allemand RABBIT, le risque de MACE a été comparé entre les JAKi et les anti-TNF chez les patients atteints de PR, et aussi comparé chez les patients à risque CV élevé (âge ≥ 50 ans et au moins un autre facteur de risque cardiovasculaire) [Y. Meissner. OP0135]
L’analyse a été réalisée sur les épisodes thérapeutiques de janvier 2017 à avril 2021, et par classe thérapeutique. L’analyse comparative a été faite avec ajustement pour l’âge, le sexe, la tabagisme, l’activité de la PR, les traitements antérieures, la corticothérapie et les comorbidités. Ont été inclus dans l’analyse : 2030 traitements par JAKi (1215 chez des patients à risque CV élevé), 2338 traitements par anti-TNF (1254 chez patients à risque CV élevé), 871 traitements de fond conventionnels (508 chez patients à risque CV élevé).
Dans le sous-groupe de patients à risque CV élevé, l’âge moyen était de 64 ans environ. Il y avait 3,1 à 3,7 comorbidités par patient. Dans la population de l’étude, il a été rapporté 28 MACE au cours du suivi.
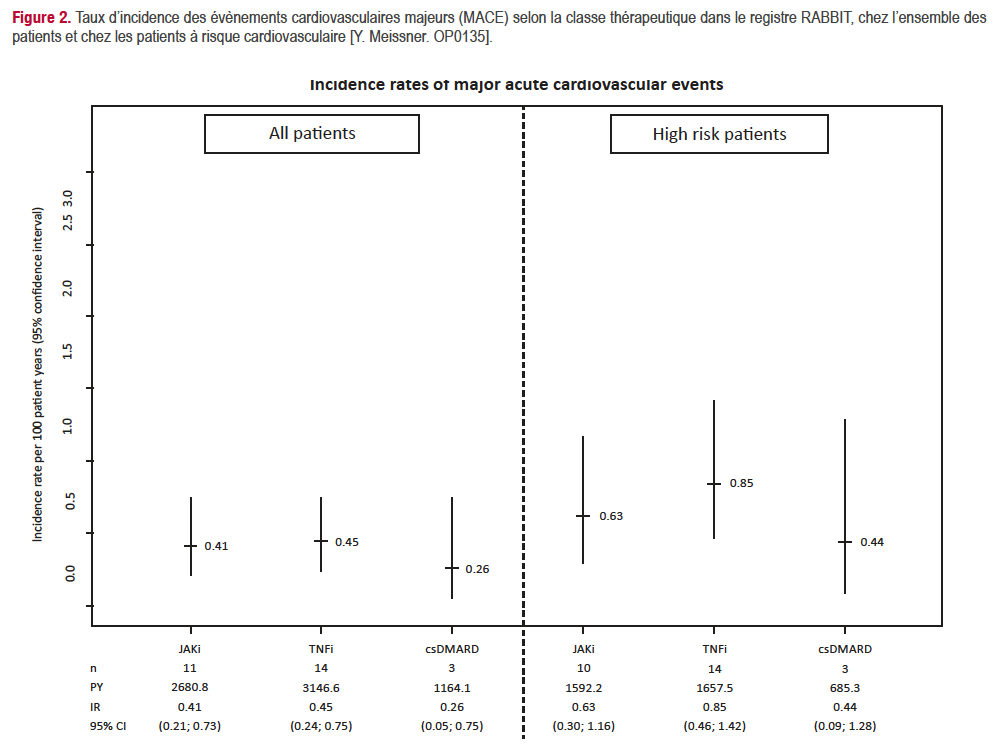
Le taux de MACE par classe thérapeutique est exposé à la figure 2. On observe qu’aussi bien dans la population de l’étude que dans le sous-groupe des patients à risque CV, il n’y a pas de différence significative entre les 3 classes thérapeutiques (avec une différence numérique en défaveur des anti-TNF). Si l’on veut comparer ces données avec ceux de l’étude ORAL surveillance, il est intéressant de noter que le taux l’incidence (pour 100 PA) des MACE sous anti-TNF dans la population à risque CV est peu différent entre les deux : 0,85 dans RABBIT, 0,73 dans ORAL surveillance.
À l’inverse, le taux d’incidence sous JAKi est de 0,63 dans RABBIT alors qu’il est de 0,91 pour la dose de 5 mg x 2/j de tofacitinib dans ORAL surveillance. Néanmoins, les populations ne sont pas les mêmes avec par exemple une plus grande prévalence de l’obésité et de la corticothérapie dans ORAL Surveillance.
La population du registre RABBIT nous apparait représentative d’une population européenne de vraie vie, ce qui n’est pas le cas de la population d’ORAL surveillance où les patients européens ne représentaient que 4 % de l’ensemble de la population. Ces résultats paraissent rassurants concernant le risque de MACE
avec la classe thérapeutique des JAKi aux doses recommandées dans la PR et dans une population européenne non sélectionnée, y compris avec des facteurs de risque CV.
| SPONDYLOARTHRITE AXIALE |
Efficacité de l’upadacitinib dans la spondyloarthrite axiale non radiographique
Pour l’instant, tous les traitements efficaces dans la spondyloarthrite axiale (ax-Spa) radiographique l’ont été dans l’axSpA non radiographique quand les pa-tients atteints de cette dernière étaient sélectionnés par l’existence d’au moins un signe objectif d’inflam-mation, à savoir une CRP augmentée ou une sacro-iliite inflammatoire à l’IRM. L’upadacitinib (UPA) est un inhibiteur de Janus Kinase (JAKi), sélectif pour JAK1, dont l’efficacité dans l’axSpA radiographique (spon-dylarthrite ankylosante) a été démontré dans l’essai de phase 2/3 SELECT-AXIS 1 (patients bio-naïfs) où la taille de l’effet versus placebo à S14 pour la réponse ASAS40 était de 26 % [van Der Heijde D. Lancet 2019 ; 394 : 2108-2017]. L’essai thérapeutique SELECT-AXIS 2, présenté àl’EULAR [Deodhar A. OP016] et publié dans le Lancet en juillet 2022 [Deodhar A. Lancet 2022 ; 400 : 369-379], est un essai de phase 3 ayant évalué l’UPA ver-sus PBO chez des patients (bio-naïfs) atteints d’une axSpA non radiographique, et présentant un signe objectif d’inflammation (CRP ultrasensible et/ou IRM).
Comme demandé dans ces essais concernant l’axSpA non radiographique par les autorités de santé amé-ricaines, la phase randomisée était de 52 semaines au cours de laquelle les patients recevaient soit l’UPA15 mg/j (n = 156), soit le PBO (n = 157). Dans la popu-lation de l’étude on comptait 58% de femmes et l’âge moyen était de 42 ans.À la semaine 14 (S14), date d’évaluation du critère prin-cipal de jugement (ASAS40), la taille de la différence entre UPA et PBO était de 22% (Réponse ASAS40 dans 45% et 23% respectivement ; p < 0,0001). La différence était également significative pour la plupart des critères de jugement secondaires à S14, notamment la faible ac-tivité ASDAS, la maladie inactive ASDAS, la qualité de vie (ASAS HI), l’évolution de la CRP et l’évolution du score SPARCC qui évalue le degré d’inflammation à l’IRM des sacro-iliaques. Il n’y a pas eu d’évènement inattendu en matière de tolérance sur cette courte période. Il faut en conclure que l’efficacité de l’UPA après 3 mois de traitement est équivalente entre l’axSpA non radio-graphique avec inflammation objective et l’axSpA radio-graphique. Ce JAKi est un nouveau traitement utilisable per os constituant un réel apport dans l’arsenal théra-peutique de l’axSpA, ce d’autant plus que son efficacité chez les patients insuffisamment répondeurs à une ou deux biothérapie (anti-TNF ou anti-IL17) a été rapportée lors du même congrès en poster, avec une taille de l’effet ASAS40 à S14 de 27% [van der Heijde D. POS0306].
Efficacité du bimékizumab dans la spondyloarthrite axiale radiographique
Le bimékizumab (BKZ) est un anticorps monoclonal anti-IL17 qui a la particularité de cibler à la fois l’IL-17A et l’IL-17F, contrairement aux anti-IL17 déjà disponibles sur le marché qui ne ciblent que l’IL-17A. On pourrait donc en espérer une efficacité supérieure. Son efficacité a été démontré dans le rhumatisme psoriasique. Dans un vaste essai de phase 2, mené avec 4 doses diffé-rentes de BKZ et publié en 2020 [van der Heijde D. Ann Rheum Dis 2020 ; 79 : 595-604], le BKZ était significati-vement supérieur au PBO à S12 pour la réponse ASAS40 chez les patients atteints d’axSpA radiographique, avec un réponse dose-dépendante. Dans l’essai de phase 3, appelé MOBILE 2 et présenté à l’EULAR [van der Heijde D. OP019], les patients atteints d’axSpA radiographique étaient soit naïfs de biothérapie, soit en échec des anti-TNF. La durée moyenne de la maladie était en moyenne de 13,5 ans et 16% des patients étaient insuffisamment répondeurs à un anti-TNF. Le BKZ était utilisé à la posologie de 160 mg toutes les 4 semaines et la phase randomisée versus PBO durait 16 semaines (332 patients randomisés). A S16, le taux de réponse ASAS40 dans le groupe BKZ était de 44,8 %, significativement supérieur à celui dans le groupe PBO qui était de 22,5 % (p < 0,001), soit une taille de l’effet de 22 % ce qui est du même ordre que celle observée avec un JAKi comme l’UPA. Les critères de jugement secondaires étaient également significativement supé-rieurs sous BKZ versus PBO, de même que l’évolution de la CRP et des signes inflammatoires aux IRM des sacro-iliaques et du rachis. Le taux des patients en rémission partielle ASAS à S16 était de 24 %. Le taux de réponse ASAS40 chez les patients insuffisamment répondeurs à un anti-TNF et traités par BKZ était de 40,5 % vs 17,6% sous PBO, soit une taille de l’effet de 22 % là encore. Parmi les patients ayant à l’inclusion un score SPARCC d’inflammation des sacro-iliaques à l’IRM supérieur à 2,38,6 % de ceux traités par BKZ étaient en rémission SPARCC à S16 versus 0 % sous PBO (le même effet favo-rable étant observé au rachis). Avec le BKZ, comme avec les autres anti-IL17 (et les autres biothérapies), le clini-cien doit connaître la possible survenue de candidoses non systémiques, comme les candidoses orales dont la fréquence était de 3,5 pour 100 patients-années dans l’extension à 3 ans de l’essai BE ACTIVE effectué dans le rhumatisme psoriasique [Coates L. Arthritis Rheumatol 2022 Jul 13, online].
Que faut-il penser de l’association anti-TNF et anti-inflammatoire non stéroïdien pour freiner la progression structurale de la spondyloarthrite axiale ?
Freiner au mieux la progression structurale chez les pa-tients atteints d’axSpA radiographique (spondylarthrite ankylosante ou SA) est un objectif qui, s’il n’est pas im-portant pour tous les patients, l’ait beaucoup pour cer-tains. Le débat, alimenté par des études, existe depuis plusieurs années entre le mérite respectif des anti-in-flammatoires non stéroïdiens (AINS), celui des anti-TNF et bientôt celui des anti-IL17. Concernant les anti-TNF, on s’accorde qu’il faut au moins 4 ans pour observer l’ef-
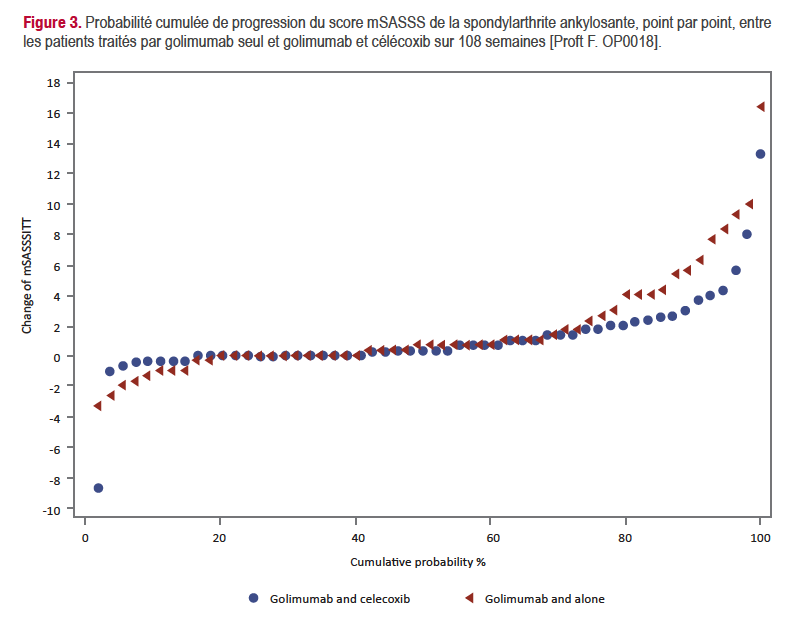
FORMATION MÉDICALE CONTINUE13COMPTE-RENDUJANVIER 2023 / LE RHUMATOLOGUE N° 112fet positif sur la progression structurale. En 2005 avait été publiés les résultats d’une étude montrant un effet positif du célécoxib (CEL) sur la progression structu-rale de la SA, mais ceci n’a pas été trouvé avec des AINS non sélectifs de la COX2 comme le diclofénac. L’idée de tester l’efficacité de l’association anti-TNF et AINS sélec-tif de la COX-2 a donc germé, aboutissant à la réalisa-tion de l’étude allemande présentée à l’EULAR [Proft F. OP0018]. Il s’agissait d’une étude d’une durée de 2 ans au cours de laquelle les patients :
• recevaient tous pendant les 12 premières semaines du golimumab (GOL) 50 mg ;
• puis ceux ayant eu une amélioration significative (amélioration du BASDAI d’au moins 2/10) étaient ran-domisés pour recevoir : soit GOL 50 mg/4s seul ; soit GOL + CEL 400 mg/j.Le nombre de patients randomisés était de 109 et ce-lui des patients ayant terminé l’étude de 97. Le critère principal de jugement était l’évolution du score radio-graphique mSASSS du rachis entre S0 et S108. Les pa-tients avaient été sélectionné initialement comme ayant un facteur de risque de progression radiographique :CRP > 5 mg/l et/ou au moins un syndesmophyte.
Le critère de jugement principal n’est pas atteint : il n’existe pas de différence significative entre GOL seul et GOL+CEL. La progression du mSASSS était de 1,1 sous GOL+CEL et de 1,7 sous GOL seul (p = 0,79). De nouveau syndesmophytes sont apparues chez 11% des patients traités par GOL+CEL et 25% de ceux traités par GOL seul (p=0,12). Ces différences ne sont pas statistiquement significatives, mais les différences numériques sont loin d’être négligeables et la différence entre les 2 groupes apparaît bien sur le graphique de probabilité cumu-lée ou chaque point représente un patient (figure 3). Le nombre de patients de l’étude est faible et il est pos-sible que les différences observées deviendraient signi-ficatives avec des effectifs supérieurs. L’utilisation d’un AINS sélectifs comme le CEL pourrait peut-être avoir un intérêt en association avec un anti-TNF chez certains patients atteints de SA et ayant une progression struc-turale rapide, ceci au moins au cours des 2 premières années de traitement.